Radioaktivität: Unterschied zwischen den Versionen
Dg (Diskussion | Beiträge) (→Weblinks) |
Dg (Diskussion | Beiträge) (→Weblinks) |
||
| Zeile 34: | Zeile 34: | ||
* [http://www.zw-jena.de/energie/kernstrahlung.html Strahlungsarten im Detail] | * [http://www.zw-jena.de/energie/kernstrahlung.html Strahlungsarten im Detail] | ||
* [http://www.geowiss.uni-hamburg.de/i-boden/lvradiop/fra_int.htm Inst. für Bodenkunde Uni Hmb.] | * [http://www.geowiss.uni-hamburg.de/i-boden/lvradiop/fra_int.htm Inst. für Bodenkunde Uni Hmb.] | ||
| − | * | + | * [http://www.lpm.uni-sb.de/chemie/begleitmaterial/Kernchemie.pdf Kernchemie] |
[[Kategorie:Physik]][[Kategorie:Chemie]] | [[Kategorie:Physik]][[Kategorie:Chemie]] | ||
Version vom 2. Februar 2007, 20:26 Uhr
Unter Radioaktivität versteht man den natürlichen Zerfall instabiler Isotope in für diese charakteristischen Zeiten, den sogenannten Halbwertzeiten.
Die Art der emittierten Strahlung bestimmt bei diesem Zerfallsvorgang die Folgeprodukte:
Inhaltsverzeichnis
Strahlungsarten

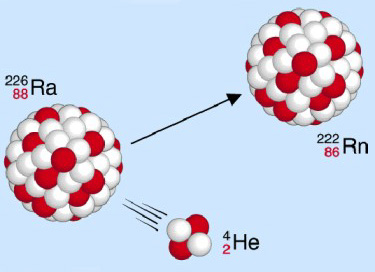
Alpha-Strahlung
Ein Alpha-Strahler emittiert Heliumkerne, somit vermindert sich für das Folgeprodukt die Massenzahl um den Wert vier, die Ordnungszahl um zwei.
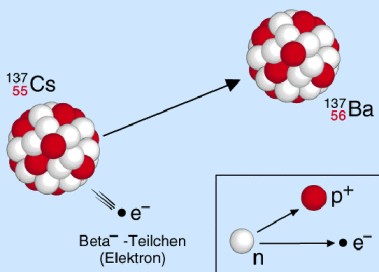
Beta-Strahlung
Beta-Strahlung hingegen besteht aus Elektronen, die durch Spaltung eines instabilen Neutrons entstehen. Damit kann für das Isotop des Folgeproduktes sowohl die Massen- als auch die Ordnungszahl errechnet werden. Hierbei gilt: die Massenzahl bleibt konstant, die Ordnungszahl erhöht sich um den Wert eins.
So zerfällt der radioaktive Beta-Strahler Kohlenstoff C-14 in das stabile Isotop N-14 des Elementes Stickstoff.